quimico
2011-10-18 13:59
Sebbene lo zinco sia disponibile in una varietà di forme, la stragrande maggioranza delle riduzioni che prevedono l'uso di zinco in acido acetico usano zinco in polvere.
Purificazione (lavaggio con acidi diluiti) è talvolta necessaria prima dell'uso, ma non sempre è di vitale importanza.
Lo zinco in acido acetico è in grado di operare un vasto range di reazioni di riduzione. Sebbene molte di queste possano essere condotte tramite l'uso di un grande numero di altri reagenti, questo reagente è di particolare valore in quanto buone chemoselettività possono spesso esser raggiunte.
Eliminazione riduttiva di eteroatomi vicinali2–15.
Una grande varietà di combinazioni di sostituenti eteroatomici sono stati eliminati riduttivamente da Zn/AcOH con successo (eq 1 e Tabella 1). Cosolventi quali etere, THF, CH2Cl2, i-PrOH, o acqua sono stati usati tutti. Le temperature di reazione variano da caso a caso, ma le rese riportate sono tipicamente buone o eccellenti.
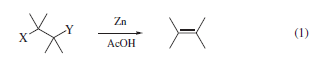 Un set di gruppi protettivi, basati sull'eliminazione usando Zn/AcOH del gruppo 2,2,2-tricloroetossi, è stata sviluppata, ed è discussa sotto come caso speciale. La Tabella 1 riporta diverse combinazioni di eteroatomi eliminati con successo sotto queste condizioni. Forse sorprendentemente, la stereochimica relativa dei due centri carboniosi non sembra permettere la trans coplanarità degli eteroatomi4,7.
Un set di gruppi protettivi, basati sull'eliminazione usando Zn/AcOH del gruppo 2,2,2-tricloroetossi, è stata sviluppata, ed è discussa sotto come caso speciale. La Tabella 1 riporta diverse combinazioni di eteroatomi eliminati con successo sotto queste condizioni. Forse sorprendentemente, la stereochimica relativa dei due centri carboniosi non sembra permettere la trans coplanarità degli eteroatomi4,7.
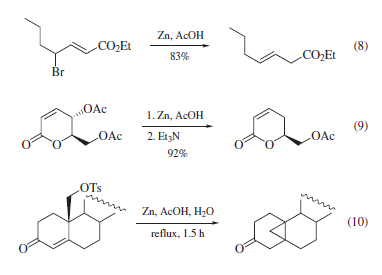
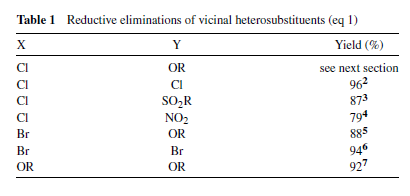 Anelli eterociclici possono esser rimossi tramite queste reazioni. Quindi, può esser ottenuta l'efficace reazione contraria di una iodolattonizzazione (eq 2)8 o di una epossidazione (dopo apertura di anello tramite ioduro) (eq 3)9.
Anelli eterociclici possono esser rimossi tramite queste reazioni. Quindi, può esser ottenuta l'efficace reazione contraria di una iodolattonizzazione (eq 2)8 o di una epossidazione (dopo apertura di anello tramite ioduro) (eq 3)9.
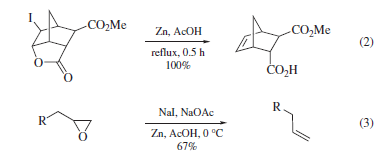 Ossime alogenate (1) eliminano a dare il nitrile con rese variabili, ma spesso buone o eccellenti (eq 4)10.
Ossime alogenate (1) eliminano a dare il nitrile con rese variabili, ma spesso buone o eccellenti (eq 4)10.
 Gruppi protettivi basati sul 2,2,2-Tricloroetossi11–15.
Sono stati sviluppati preziosi gruppi protettivi per alcoli11, fenoli11c, amine11c ed acidi carbossilici12, ed un reagente di introduzione/protezione per tioli13, tutti dipendenti dalla labilità di questo gruppo alle eliminazioni riduttive con Zn/AcOH. Esse sono riassunte nella Tabella 2.
Gruppi protettivi basati sul 2,2,2-Tricloroetossi11–15.
Sono stati sviluppati preziosi gruppi protettivi per alcoli11, fenoli11c, amine11c ed acidi carbossilici12, ed un reagente di introduzione/protezione per tioli13, tutti dipendenti dalla labilità di questo gruppo alle eliminazioni riduttive con Zn/AcOH. Esse sono riassunte nella Tabella 2.
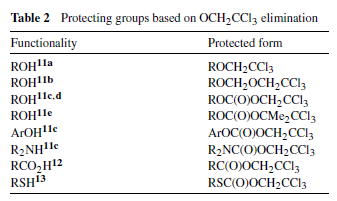 Il tricloroacetilidene acetale è anche stato proposto come potenziale protezione per i dioli, e da deproteggersi in modo simile14. È stata proposta, insieme a simili metodi, la protezione di amine come 2-iodoetil carbammato, da deproteggersi poi con Zn polvere in MeOH15 ma ha trovato un utilizzo davvero piccolo.
Scissione eteroatomo–eteroatomo16–27
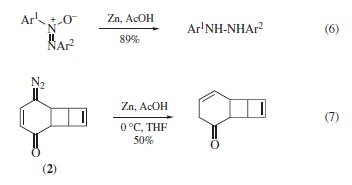
I doppi legami N=N possono esser scissi16 da Zn/AcOH; meno frequentemente, le idrazine17 possono essere ottenute dalla riduzione (eqs 5 and 6)17. Gli idrazoni possono anche esser ridotti ad amine18, come possono esser usate18b in una variante della classica sintesi di Knorr dei pirroli. Il diazo chetone (2) è stato ridotto con successo, nonostante l'apparente potenziale per reazioni secondarie sconvenienti (eq 7)19.
Il tricloroacetilidene acetale è anche stato proposto come potenziale protezione per i dioli, e da deproteggersi in modo simile14. È stata proposta, insieme a simili metodi, la protezione di amine come 2-iodoetil carbammato, da deproteggersi poi con Zn polvere in MeOH15 ma ha trovato un utilizzo davvero piccolo.
Scissione eteroatomo–eteroatomo16–27
I doppi legami N=N possono esser scissi16 da Zn/AcOH; meno frequentemente, le idrazine17 possono essere ottenute dalla riduzione (eqs 5 and 6)17. Gli idrazoni possono anche esser ridotti ad amine18, come possono esser usate18b in una variante della classica sintesi di Knorr dei pirroli. Il diazo chetone (2) è stato ridotto con successo, nonostante l'apparente potenziale per reazioni secondarie sconvenienti (eq 7)19.
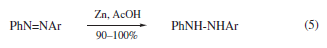
 I nitro gruppi aromatici20a (quelli alifatici possono condurre ad ossime20b, anche se non tutte dovrebbero esser stabili sotto tutte le condizioni di reazione), le idrossilamine21, le ossime22 (ancora una volta, trovano uso22b in una sintesi pirrolica di Knorr), le N-nitro-23a e le N-nitrosoamine23b, N-ossidi aromatici24 e legami aromatici N–S25 sono stati tutti ridotti ad amine con Zn/AcOH. Questi riferimenti provano l'ampia evidenza della capacità di questo reagente di compiere la reazione desiderata, mentre lascia intatto, per esempio, bromuri22, atomi di zolfo legati a carbonio20,23b e doppi legami C=C isolati21. Naturalmente, le amine da poco liberate subscono reazioni intramolecolari spontanee.
Le solfonamidi26 possono anche esser ridotte a tioli.
Lo Zn in AcOH può agire come utile reagente alternativo per il workup riduttivo delle reazioni di ozonolisi27, che possono esser considerate, almeno formalmente, coinvolgere la scissione del legame O–O.
Curiosamente, la forza delle condizioni riportate per poter condurre queste diverse reazioni sono sembra seguire alcun cammino costante; le condizioni di reazione, quindi, possono aver bisogno di un determinazione individuale in molti casi.
I nitro gruppi aromatici20a (quelli alifatici possono condurre ad ossime20b, anche se non tutte dovrebbero esser stabili sotto tutte le condizioni di reazione), le idrossilamine21, le ossime22 (ancora una volta, trovano uso22b in una sintesi pirrolica di Knorr), le N-nitro-23a e le N-nitrosoamine23b, N-ossidi aromatici24 e legami aromatici N–S25 sono stati tutti ridotti ad amine con Zn/AcOH. Questi riferimenti provano l'ampia evidenza della capacità di questo reagente di compiere la reazione desiderata, mentre lascia intatto, per esempio, bromuri22, atomi di zolfo legati a carbonio20,23b e doppi legami C=C isolati21. Naturalmente, le amine da poco liberate subscono reazioni intramolecolari spontanee.
Le solfonamidi26 possono anche esser ridotte a tioli.
Lo Zn in AcOH può agire come utile reagente alternativo per il workup riduttivo delle reazioni di ozonolisi27, che possono esser considerate, almeno formalmente, coinvolgere la scissione del legame O–O.
Curiosamente, la forza delle condizioni riportate per poter condurre queste diverse reazioni sono sembra seguire alcun cammino costante; le condizioni di reazione, quindi, possono aver bisogno di un determinazione individuale in molti casi.
I seguenti utenti ringraziano quimico per questo messaggio: AgNO3, rock.angel, jobba, zodd01, Hamiltoniano
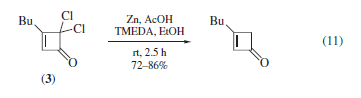
 La scissione in α al gruppo carbonile è stata sfruttata nell'uso del gruppo protettivo fenacile34. La riduzione di composti quali ad esempio il (3) ritiene l'anello a quattro membri tensionato, e spesso porta ad eccellenti rese (eq 11)31c.
La scissione in α al gruppo carbonile è stata sfruttata nell'uso del gruppo protettivo fenacile34. La riduzione di composti quali ad esempio il (3) ritiene l'anello a quattro membri tensionato, e spesso porta ad eccellenti rese (eq 11)31c.
 Riduzione del carbonile35–37.
I chinoni vengono ridotti ad idrochinoni tramite Zn/AcOH a riflusso35a. L'inserimento di Ac2O nella miscela di reazione conduce al rispettivo diacetato35a. In condizioni più blande (temperatura ambiente), l'intermedio γ-idrossicicloesenone può esser intercettata con rese sorprendentemente elevate (72–90%)35b.
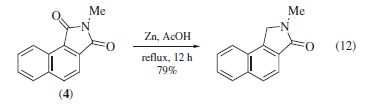
I diaril chetoni possono esser ridotti ad alcoli36a ma è anche stata riportata una dimerizzazione competitiva36b in alcuni casi insoliti. La riduzione della ftalimide (4) procede bene e, specialmente, con regiospecificità (eq 12)37.
Riduzione del carbonile35–37.
I chinoni vengono ridotti ad idrochinoni tramite Zn/AcOH a riflusso35a. L'inserimento di Ac2O nella miscela di reazione conduce al rispettivo diacetato35a. In condizioni più blande (temperatura ambiente), l'intermedio γ-idrossicicloesenone può esser intercettata con rese sorprendentemente elevate (72–90%)35b.
I diaril chetoni possono esser ridotti ad alcoli36a ma è anche stata riportata una dimerizzazione competitiva36b in alcuni casi insoliti. La riduzione della ftalimide (4) procede bene e, specialmente, con regiospecificità (eq 12)37.
 Riduzione di alcheni attivati38–40.
La sostituzione con un carbonile (mono-38a o di-38b) rende un doppio legame C=C soggetto a riduzione tramite Zn/AcOH. α,β,γ,δ-Dienoni possono portare o a α,β-38a o a β,γ-enoni38c in rese in entrambi casi elevate. Una recente modificazione39 a più bassa temperatura (t.a.), e con tempi di reazione molto più corti, usa ultrasonicazione; sono state raggiunte rese eccellenti.
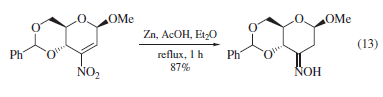
Possono anche esser ridotti nitro composti α,β-insaturi40. In condizioni più blande un'ossima può esser ottenuta (eq 13)40a; una reazione più vigorosa porta al corrispondente chetone40b.
Riduzione di alcheni attivati38–40.
La sostituzione con un carbonile (mono-38a o di-38b) rende un doppio legame C=C soggetto a riduzione tramite Zn/AcOH. α,β,γ,δ-Dienoni possono portare o a α,β-38a o a β,γ-enoni38c in rese in entrambi casi elevate. Una recente modificazione39 a più bassa temperatura (t.a.), e con tempi di reazione molto più corti, usa ultrasonicazione; sono state raggiunte rese eccellenti.
Possono anche esser ridotti nitro composti α,β-insaturi40. In condizioni più blande un'ossima può esser ottenuta (eq 13)40a; una reazione più vigorosa porta al corrispondente chetone40b.
 Contrazione di anelli aza-eterociclici.
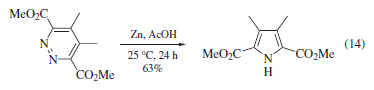
Una varietà di poliaza eterocicli a sei membri subiscono contrazione con formale rimozione di N, ad esempio eq 1441a. Altri eteroatomi nell'anello sono tollerati: 1,2,3-triazine portano a pirazoli41b e 1,2,4-triazines portano ad imidazoli41c, con questi ultimi che di solito richiedono temperature di riflusso.
L'utilità della sintesi indolica da cinnoline41d tramite questo metodo dovrebbe esser notata. L'adiacenza degli eteroatomi non è richiesta: le conversioni di pirimidina a pirrolo42a,b e della 1,3,5-triazina ad imidazolo42c sono state registrate. Il meccanismo di queste conversioni non è chiaro, ma si ritiene siano coinvolti diidro derivati ciclici41a,42b.
Contrazione di anelli aza-eterociclici.
Una varietà di poliaza eterocicli a sei membri subiscono contrazione con formale rimozione di N, ad esempio eq 1441a. Altri eteroatomi nell'anello sono tollerati: 1,2,3-triazine portano a pirazoli41b e 1,2,4-triazines portano ad imidazoli41c, con questi ultimi che di solito richiedono temperature di riflusso.
L'utilità della sintesi indolica da cinnoline41d tramite questo metodo dovrebbe esser notata. L'adiacenza degli eteroatomi non è richiesta: le conversioni di pirimidina a pirrolo42a,b e della 1,3,5-triazina ad imidazolo42c sono state registrate. Il meccanismo di queste conversioni non è chiaro, ma si ritiene siano coinvolti diidro derivati ciclici41a,42b.
 Riduzioni di sostituenti arilici.
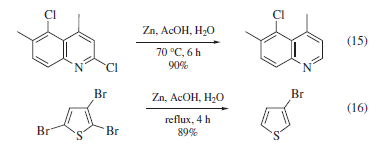
Sebbene, come menzionato sopra, molte funzionalità potenzialmente labili siano stabili in presenza di Zn/AcOH, gli ioduri arilici possono essere dealogenati43. La sostituzione di Cl o Br in posizione 2 in composti eteroatomici li rende anche soggetti a riduzione, spesso con eccezionale selettività (eqs 15 and 16)44.
Riduzioni di sostituenti arilici.
Sebbene, come menzionato sopra, molte funzionalità potenzialmente labili siano stabili in presenza di Zn/AcOH, gli ioduri arilici possono essere dealogenati43. La sostituzione di Cl o Br in posizione 2 in composti eteroatomici li rende anche soggetti a riduzione, spesso con eccezionale selettività (eqs 15 and 16)44.
 Sono 1po' come la luce: dualismo onda-particella
Sono 1po' come la luce: dualismo onda-particella 