quimico
2012-11-23 19:18
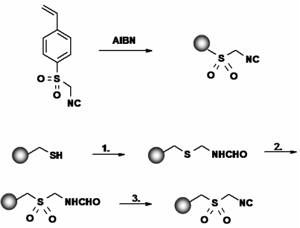
La chimica del TOSMIC è stata elaborata in maniera esaustiva dal chimico olandese Prof. van Leusen e dalla sua scuola. Esso costituisce in assoluto il più versatile sintone derivato dal metile isonitrile ed esibisce un chimica poliedrica che è di grande utilità in sintesi organica. Il TOSMIC costituisce un building block densamente funzionalizzato con tre gruppi cruciali che contribuiscono ad una varietà di reazioni (Fig. 1): la funzione isonitrile subisce le tipiche reazioni di α-addizione, l'atomo di carbonio α acido, ed il gruppo sulfonile in posizione α che ha due funzioni, agire sia da gruppo uscente sulfinile e aumentare ulteriormente l'acidità del carbonio α. I gruppi geminali isonitrile e tosile nel TOSMIC possono essere considerati come un speciale tipo di acetale-N,S, e reagiscono di conseguenza.
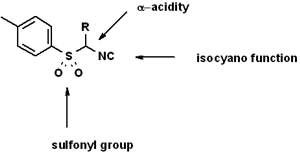
Figura 1
Il TOSMIC è un reagente di sintesi polivalente (Fig. 2). Esso effettua cianazioni riduttive di chetoni ed aldeidi, e facilmente subisce condensazioni tipo Knoevenagel con aldeidi e chetoni. Il reagente è un sintone connettivo C1 e può essere inoltre dialchilato. Oltretutto, dato che è un derivato eteroacetalico, è utile per la sintesi di chetoni tramite alchilazione e successiva idrolisi. Questo processo costituisce un Umpolung della reattività della formaldeide.
Nella sintesi di eterocicli, esso fornisce una versatile sintesi di ossazilidinoni ed ossazoli, tiazoli, imidazoli, indoli, triazoli e pirroli (Fig. 2).
Oggi, sono commercialmente disponibili molti altri derivati del TOSMIC α-sostituiti oltre al composto genitore, facilitando quindi il suo uso in chimica applicata e combinatoriale. La chimica del TOSMIC è stata recentemente esposta in modo autorevole in una review apparsa su Organic Reactions (D. van Leusen, A. M. van Leusen, Org. React. 2003, 57, 419).
Questa piccola review mira ad evidenziale alcune applicazioni recenti delle reazioni multicomponente (MCRs) basate sul TOSMIC.
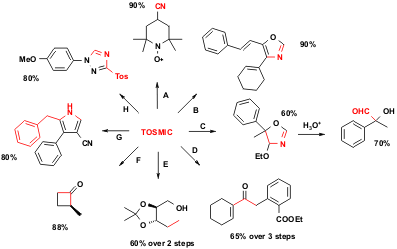
Figura 2 La parte in rosso mostra le porzioni del prodotto che derivano dal materiale di partenza TOSMIC.
A (Cianazione riduttiva, selettiva, di chetoni): TOSMIC, t-BuOK;
B (Formazione dell'anello ossazolico): 1. Condensazione del TOSMIC con cicloesanone, 2. aldeide cinnamica, 2 eq. n-BuLi (-70 to 0 °C, 2 h);
C (Formazione della 4-alcossi-2-ossazolina): 1. acetofenone, TOSMIC, EtOH; 2. H3O+;
D (Formazione di chetoni α,β-insaturi sostituiti): 1. Condensazione del TOSMIC con cicloesanone, 2. benzil bromuro, t-BuOK, DME; 3. H3O+;
E (TOSMIC come reagente connettivo, riduzione): 1. alchil ioduro, TOSMIC, PTC, 2. Li, NH3(liq.);
F (TOSMIC come reagente connettivo, idrolisi): 1. TOSMIC, dialchilazione 2. H2SO4 (50%), sulfolano, da 20 a 100 °C, 2 h;
G (Pirroli da accettori di Michael): TOSMIC benzil sostituito, NaH, acrilonitrile;
H (Formazione di triazoli): Sale di diazonio, TOSMIC, K2CO3, DMSO, MeOH, H2O, -10 °C.
Imidazoli 1,4,5-trisostituiti tramite vL-3CR
Oltre alla classiche reazioni di Passerini ed Ugi, la chimica di van Leusen del TOSMIC e dei suoi derivati costituisce la più importante applicazione delle reazioni multicomponente di isonitrili (IMCR). Nel 1977, van Leusen descrisse la reazione di aldeidi, amine primarie e TOSMIC, ottenendo così imidazoli 1,4,5-trisostituiti (vL-3CR) che non sono in altro modo ottenibili (A. M. van Leusen, J. Wildeman, O. H. Oldenziel, J. Org. Chem. 1977, 42, 1153. A. M. van Leusen, Heterocycl. Chem. 1980, 5, S-111). Il meccanismo implica la cicloaddizione del TOSMIC ad una base di Schiff, un doppio legame carbonio-azoro, una ciclizzazione indotta da base e un riarrangiamento di protone verso un'imidazolina, che subito dopo aver perso acido tosilsulfinico aromatizza a dare un imidazolo. La reazione procede in solventi protici o non protici polari (EtOAc, THF, MeCN, DMF, DCM, MeOH), da t.a. a reflusso, molto spesso in condizioni anidre. n-BuLi, t-BuOK ed NaH sono stati descritti come base richiesta; ma la reazione è stato trovato anche aver bisogno di una base blanda per promuovere la cicloaddizione (piperazina, morfolina, K2CO3). La scelta della condizioni di reazione è influenzata dalla solubilità dell'aldeide e dell'amina così come dall'isolamento del prodotto. La combinazione di DMF/K2CO3 è descritta come la scelta migliore per assicurarsi cicloaddizioni TOSMIC/immina riuscite. Comunque, altre combinazioni di solvente/base possono essere allo stesso modo efficaci e posso aiutare ad evitare la difficoltà associate alla rimozione della DMF dal prodotto.
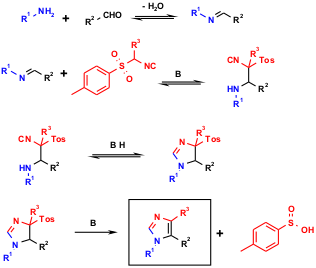
Figura 3
La maggior parte degli esempi pubblicati finora hanno usato immine che sono prive di alcuna funzionalità addizionale. Solo recentemente l'utilità di questa reazione è stata drammaticamente aumetata tramite l'introduzione e l'indagione di TOSMIC α-sostituiti e di una varietà di gruppi funzionali nei materiali di partenza. Sisko et al. della Glaxo-Smith-Kline investigarono scopo e limitazioni approfondite di questa sintesi imidazolica (J. Org. Chem. 2000, 65, 1516. DOI: 10.1021/jo991782l).
Inoltre fu scoperto che la reazione lavora abbastanza bene con aldeidi che recano altri gruppi O-funzionali in diversi stati di ossidazione, come il gliossale che porta ad un gruppo aldeidico libero nel prodotto 11, l'idrossiacetaldeide che porta ad un gruppo idrossile primario libero nel prodotto 12, α-chetoaldeidi che portano a gruppi chetonici liberi nei prodotti 10 e 16 o esteri 13. Inoltre, sono ben tollerati gruppi fenolici liberi 15 o gli eterocicli indolo 14, imidazolo e piridina, come in 13 e 16 rispettivamente.
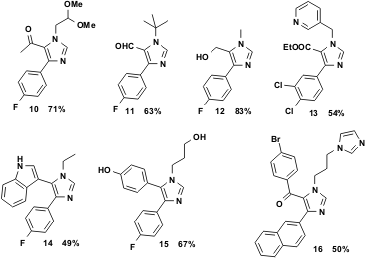
Figura 4
Anche dialdeidi e diamine sono state usate con successo in questa reazione multicomponente per generare bis-imidazoli dimerici. La dialdeide glutarica, come soluzione acquosa al 50%, rapidamente reagisce con un'amina a formare il bis-imidazolo 17. Inoltre, l'idrogenoliticamente sensibile cisteamina reagisce bene a dare il corrispondente bis-imidazolo 18 con una resa eccellente.
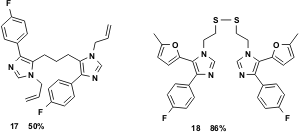
Figura 5
Un'altra famiglia di molecole target attraenti per la metodologia vL-3CR sono gli acidi 2-imidazol-1-il alcanoici. È stato dimostrato che gli α- ed i β-amino acidi non protetti sono buoni substrati in questa reazione. Inoltre gli α-amino acidi chirali portano ai prodotti otticamente puri 19-21.
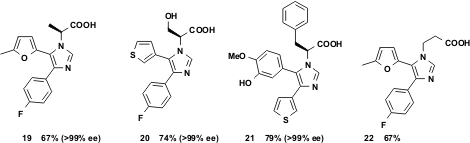
Figura 6
L'acido gliossilico può essere usato in modo vantaggioso come sostituto della formaldeide, e conduce agli imidazoli 1,4-disostituiti 23-25 con rese elevate. Si assume che non appena aver aggiunto la base e il TOSMIC, la base di Schiff decarbossili. I corrispetti imidazoli 4,5-disostituiti sono anche accessibili usando la vL-3CR. Quindi, trattando semplicemente un'aldeide con un eccesso di NH4OH (acquoso, 30%) in THF, e aggiungendo un isonitrile, si generano gli imidazoli 26-29 in una singola operazione.
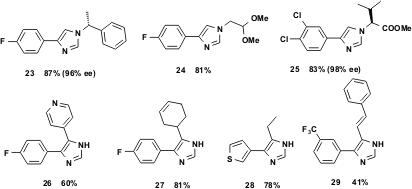
Figura 7
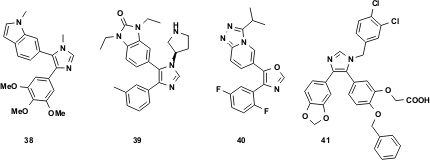
Fuori dalla classe degli imidazoli 1,4,5-trisostituiti, è stato scoperto un potente e selettivo inibitore della chinasi p38 37 (J. Sisko, M. Mellinger, P. W. Sheldrake, N. H. Baine., Tetrahedron Lett. 1996, 37, 8113. DOI: 10.1016/0040-4039(96)01886-2). Questo composto ha possibili implicazioni nel trattamento dell'artrite reumatoide e lo sviluppo è stato successivamente promosso alla fase III dei trials clinici. Quindi, è stata sviluppata una preparazione tecnica di quantità dell'ordine dei kg (J. Sisko, M. Mellinger, Pure Appl. Chem. 2002, 74, 1349.). La sintesi del derivato del TOSMIC sulla scala di diverse centinaia di kg è mostrata in Figura 8. Il corrispondente precursore TOSMIC, la formammide 33, è stato sintetizzato impiegando un'altra reazione multicomponente, una α-amino alchilazione della p-fluorobenzaldeide (30), formammide (31) e acido p-metilfenilsulfinico (32) in presenza di TMSCl in toluene. La disidratazione è semplice da fare, sperimentalmente comporta l'addizione di un eccesso di Et3N ad una sospensione della formammide in THF contenente due equivalenti di POCl3 (metodo di Ugi). Non appena isolato, il derivato del TOSMIC è un materiale stabile cristallino, facilmente maneggiabile. Questa sintesi è stata usata per produrre in eccesso di 500 kg 34 senza problemi.
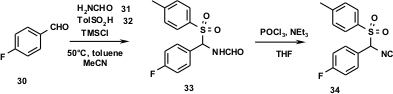
Figura 8
La sintesi tecnica su larga scala dell'inibitore finale 37 è mostrata nella Figura 9. La vL-3CR e le successive trasformazione del gruppo protettivo portano alla chiara formazione dell'imidazolo 37 con una resa isolata del 60–65%, anche su una scala di 200 galloni.
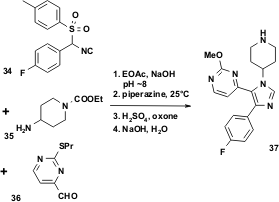
Figura 9
I seguenti utenti ringraziano quimico per questo messaggio: rock.angel, Hegelrast