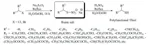
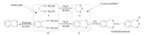
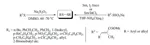
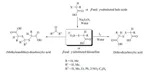
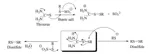
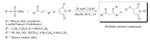
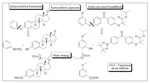
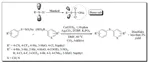
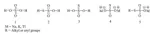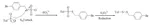Un tiolo è un composto organozolfo dal cattivo odore [24, 25] (analogo allo zolfo di un alcole) contenente un legame carbonio-zolfo (R-SH) (dove R può essere un sostituente alchilico o arilico) [26, 27]. I metodi di laboratorio per la sintesi di tioli sono stati riportati in molti studi [28 - 31]. Vermeulen ed il suo gruppo hanno sviluppato un efficiente strumento combinatorio per la preparazione di nuovi composti modificatori di aroma [32]. Essi hanno usato i sali di Bunte per la preparazione di tioli polifunzionalizzati. I tioli polifunzionalizzati non sono così ben noti ed è raro siano disponibili commercialmente [33 - 35]. Possono essere spesso instabili quando esposti alla luce, ad alte temperature o a condizioni ossidative ed è molto difficile isolarli usando le comuni tecniche estrattive o detector GC. Lo scopo principale del loro lavoro fu quello di trovare un ulteriore cammino sintetico per sintetizzare e caratterizzare nuovi tioli polifunzionalizzati. Venti tioli polifunzionalizzati sono stati ottenuti usando l'approccio di sintesi combinatorio one-pot come mostrato nello Schema 3 [32].
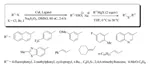
Gli aril tioli sono difficili da sintetizzare comparati alle controparti alifatiche [36 - 38]. La formazione in-situ del sale di Bunte attraverso la reazione catalizzata da Pd di aril bromuri con sodio tiosolfato in presenza di Cs2CO3 seguita dalla riduzione del risultante sale di Bunte con Zn/HCl forniva praticamente una resa eccellente di aril tioli. Questo metodo è interessante a causa del baso costo e delle facile disponibilità di aril bromuri e cloruri rispetto agli aril ioduri [39].
Reeves et al. hanno descritto una metodologia semplice e pulita per la sintesi di solfuri da sali di Bunte (S-alchile, S-arile ed S-vinile) e reattivi di Grignard. I sali di Bunte S-alchile sono stati preparati attraverso semplice reazione SN2 tra un alogenuro alchilico e sodio tiosolfato mentre i sali di Bunte S-arile/S-vinile sono stati preparati attraverso coupling catalizzato da Cu di alogenuri arilici/vinilici con tiosolfati di sodio. Uno schema generale per la preparazione dei sali di Bunte e la reazione dei sali di Buinte con i reattivi di Grignard sono presentati negli Schemi 4 e 5 [12].
La sintesi dei solfuri tramite reazione dei sali di Bunte e i reattivi di Grignard è un approccio pulito dal punto di vista ambientale a causa delle seguenti ragioni: (a) nessun tiolo viene usato per la sintesi di solfuri, (b) si forma come sottoprodotto un solfito inodore, (c) questo processo ha il vantaggio di essere prontamente disponibile, di essere commercialmente vantaggio, di poter preparare in situ i composti dagli alogenuri corrispondenti, di avere a disposizione una vasta scelta di reattivi di Grignard [12].
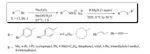
La formazione di aril tioeteri catalizzata da metallo ha certamente degli svantaggi, perché durante la reazione, una quantità quantificabile di disolfuro viene formata in condizioni aerobiche. Jiang et al. hanno evidenziato le proprietà mascherate dello ione SO3– in condizioni di cross-coupling ossidative [40]. La formazione del disolfuro è stata soppressa in maniera efficace attraverso una strategia mascherata in atmosfera di CO2. Essi hanno descritto il cross-couplig ossidativo diretto catalizzato da Cu inodore tra acidi boronici e solfuri mascherati recanti tioeteri. Un'ampia gamma di acidi boronici, sali di Bunte e processi scalabili ne indicano la praticità (Schema 6). Questa metodologia è stata ulteriormente applicata alla modifica di farmaci in fase avanzata alla sintesi asimmetrica di dibenzotiofeni (DBTs). In questo lavoro, lo ione SO3– è stato scelto come candidato giusto per il mascheramento a causa delle sue eccezionali proprietà: i) un gruppo elettron-attrattore previene la forte coordinazione col metallo; ii) un gruppo ingombrato previene la formazione di disolfuri e iii) un gruppo coniugato modera l'elettrone.
Questo metodo è stato prontamente applicato alla diversificazione di farmaci in fase avanzata (Schema 7) [41 - 43]. L'Estratriene modificato con zolfo ed il Fenofibrat decorato con zolfo sono stati efficacemente sintetizzati e lo schema sintetico è illustrato attraverso l'approccio retrosintetico per una migliore comprensione.
La reazione di coupling decarbossilativo [44 - 47] è una interessante strategia sintetica per la costruzione di legami C-C e C-eteroatomo [48]. In questo caso, l'acido alchinil carbossilico è una buona scelta come substrato. È stata riportata una formazione di un legame C-X (X = S, Se) senza tioli tramite coupling catalizzato da Cu decarbossilativo di acidi alchinil carbossilici con sali di Bunte [49]. Questa metodologia è applicabile a vari acidi alchinil carbossilici e sali di Bunte ed è abbastanza tollerata da una vasta varietà di gruppi funzionali. Il legame C-Se può anche essere costruito con seleno sali di Bunte. Il ruolo dell'Ag2CO3 in questo protocollo è di ossidare il Cu(I) a Cu(II) così che il sale di Bunte resti attaccato alla specie Cu(II) in questo ciclo catalitico [49].
L'ossidazione dei sali di Bunte insaturi in presenza di iodio è stata stabilita da Riekes et al. Essi mostrarono che l'ossidazione del pent-4-enil tiosolfato con iodio in acqua-etanolo a riflusso produceva 2-(etossimetil)-tetraidrotiofene, 7 e 2-(idrossimetIl)-tetraidrotiofene, 8 invece del pentenil disolfuro. Il cammino meccanicistico considerato fu l'ossidazione del sale di Bunte da parte dello iodio a formare sulfenile ioduro seguita dalla addizione intramolecolare a dare lo ione epi-solfonio (Schema 8). Il risultante ione epi-solfonio veniva convertito nei prodotti attraverso l'attacco dello ione solvente. La possibilità di una via radicalica è stata esclusa e questo è stato dimostrato da u esperimento di trapping fenolico [50].
Un efficace iodio privo di metalli che catalizza la sintesi di 3-tioindoli è stato sviluppato con successo da sali di Bunte inodori, cristallini, stabili e prontamente disponibili come agenti sulfenilanti da Qi et al. Questo metodo è stato scoperto essere benigno per l'ambiente in termini di fonti di zolfo, catalizzatore e solvente. La reazione catalitica era selettiva per la posizione C-3 degli indoli e compatibile per un'ampia gamma di substrati. I sali di Bunte sono stati convertiti in un elettrofilo reattivo, ad es. ioduro di sulfenile (RSI) tramite reazione con iodio [51]. Il risultante ioduro di sulfenile è molto incline a subire la reazione di sostituzione elettrofila con indoli. Lo schema generale di reazione e il meccanismo probabile sono presentati nello schema 9 [51].
La sulfenilazione di indoli in condizioni prive di metalli e in condizioni senza ossidante è stata ottenuta da Ji et al. Il sale di Bunte è stato usato come agente sulfenilante e nel corso della reazione è stato ossidato a disolfuro. Quindi il disolfuro ha reagito con I2, generato da n-Bu4NI a dare sulfenile ioduro. Nell'ultimo passaggio, l'indolo ha reagito con sulfenile ioduro a dare dei derivati indolici sulfenilati in posizione 3 [52].
Un metodo diretto ed efficiente per la reazione di acetamidosulfenilazione di alcheni fu sviluppata da Lin e collaboratori. In questa metodologia NaI fu usato come catalizzato al posto di I2 ma DMSO agiva come ossidante. Una reazione blanda senza metalli di alchene, sale di Bunte e nitrile/alcole in presenza di NaI ed un ossidante ha fornto i seguenti composti in buone rese (Schema 10) [53].
Il miglioramento di metodi blandi e generali per la formazione di un legame C-S [54 - 56] ha ricevuto un significativo interesse poiché il legame C-S è davvero cruciale in molti composti biologici e farmaceutici. In precedenza, la sintesi dei legami C-S è generalmente effettuata tramite una reazione di condensazione tra un tiolato metallico e un alogenuro organico. La formazione del legame C-S è stata ottenuta con l'aggiunta di sali di Bunte come precursori dei tioli e composti carbonilici α,β-insaturi. Lu et al. ha sviluppato un metodo, un approccio utile per la sintesi di composti β-sulfido carbonilico da una miscela economica, inodore di sodio tiosolfato e alogenuri alchilici o sali di Bunte come surrogati alternativi ai tioli. Diversi catalizzatori acidi sono stati usati per l'ottimizzazione, ma fu scoperto che un 20 mol% di TsOH era il migliore sistema catalitico. Diversi composti carbonilici α,β-insaturi inclusi calconi, benzilidine acetone hanno reagito con i sali di Bunte in presenza di TsOH e metanolo a dare i corrispondenti prodotti. Fu trovato che i sale di Bunte benzilici, allilici e cicloesilici erano reattivi in eguale modo in questo protocollo. Ma i sali di Bunte cicloesilici davano una resa minore del prodotto a causa di ragioni steriche. I sali di Bunte ossicarbonilmetilici non davano i prodotti desiderati a causa di una reazione di transesterificazioni parassita. Questa metodologia è stata anche efficace per sistemi maleimmidici N-sostituiti. Inoltre, le condizioni di reazione sono state ottimizzate conducendo una reazione multi-componente one-pot di benzile cloruro, Na2S2O3 e composti carbonilici α,β-insaturi in una metodica multi-componente. Questo processo dava anche il prodotto desiderato ma richiedeva una quantità in eccesso di substrati e uno spreco non necessario di questi materiali (Schema 11) [57].
Milligan e Swan svilupparono una metodologia per la facile sintesi di disolfuri utilizzando sali di Bunte e tiourea in un mezzo acido. Il meccanismo della reazione è riportato di seguito (Schema 12) [58].
L'uso di sali di Bunte per la preparazione diretta di acidi dicarbossilici che sono disolfuri, mercaptali e mercaptoli è stato discusso da Stoner e dal suo gruppo. In questo procedimento, è stata discussa la conversione del disodio S-carbossimetil tiosolfato in acido ditiodiacetico in presenza di iodio e acqua. Analogamente, con questo metodo sono stati ottenuti anche acidi α, α/-, β, β/-ditiodipropionici e γ, γ/-ditiodibutirrici. Anche gli acidi dibasici del tipo tioacetale sono stati preparati direttamente a partire da composti carbonilici e da acidi alifatici sostituiti da alogeni in presenza di sali di Bunte (Schema 13) [59].
Un approccio green e senza metalli per la sintesi di disolfuri simmetrici è stato riportato da Abbasi e collaboratori. In questa metodologia, i disolfuri simmetrici dai loro corrispondenti alogenuri primari, secondari, allilici e benzilici sono stati preparati in DMSO a 60-70 °C. Il DMSO gioca un duplice ruolo in questa reazione: agisce da solvente adatto per la reazione oltre che come agente ossidante proprio per i tioli [60] (Schema 14).
Inoltre, i disolfuri simmetrici possono essere sintetizzati quando i sali di Bunte sono stati trattati con samario in presenza di indio(III) cloruro [61], o iodio molecolare (Schema 14) [62].
Molto recentemente Jiang et al. hanno sviluppato un processo redox a base di zolfo tra sulfinato e tiosolfato, che forniva in modo efficiente diversi disolfuri asimmetrici. Tramite questo nuovo metodo, la modifica di prodotti farmaceutici e naturali può essere fatto senza il bisogno di nessun altro ossidante addizionale o riducente. In questo protocollo di reazione, i cloruri alchilici prima reagivano con sodio tiosolfato formando il sale di Bunte, quindi il sodio 4-metilbenzenesulfinato veniva aggiunto alla miscela di reazione e scaldato a riflusso per 11 h. Una varietà di disolfuri asimmetrici fu ottenuta tramite questo processo. L'operazione sulla scala dei grammi è stata anche fatta per esaminare l'utilità pratica. Il meccanismo SN2 proposto nello Schema 15 è stato suggerito da esperimenti di controllo [63].
Czerwinski e il suo gruppo hanno eseguito uno studio di voltammetria ciclica sull'adsorbimento e l'ossidazione dei sali di Bunte dei prodotti di reazione elettrodica su elettrodi di oro e platino, rispettivamente. Per il confronto dello studio, hanno effettuato gli esperimenti singolarmente in soluzioni basiche (1 M NaHCO3) e acide (0,5 M H2SO4). Durante gli esperimenti, le soluzioni sono state deossidate facendo passare l'azoto attraverso la cella. Due sali di Bunte, vale a dire C6H13-SSO3Na (R è una catena alifatica) e C6H5CH2-SSO3Na (R è una catena aromatica) sono stati presi per questo studio. Lo studio di voltammetria ciclica con elettrodi di oro e platino è stato fatto separatamente. I sali di Bunte sono stati prima adsorbiti sulla superficie del metallo e poi ossidati a disolfuri. L'effetto dell'aumento delle correnti di ossidazione con un aumento della concentrazione del composto durante l'agitazione della soluzione implica che i sali di Bunte sono stati ossidati in disolfuri dalla massa della soluzione (Schema 16) [1].
I trisolfuri organici [64, 65] sono molecole molto importanti e presenti in molte fonti naturali, in particolare nelle piante della famiglia delle cipolle (genere Allium) [66, 67]. Diversi prodotti naturali, l'allimetil trisolfano [68], il trisolfuro misto tra cisteina e glutatione [69] e la sporidesmina [70] contengono ponti trisolfuro. Alcuni metodi comuni per la sintesi dei trisolfuri organici sono stati riportati in letteratura [71 - 73]. Tra questi metodi, i trisolfuri di dialchile possono anche essere ottenuti dalla reazione di sodio S-alchil tiosolfato (sali di Bunte) con solfuro di sodio a pH 8 (schema 17).
Milligan e Swan hanno descritto un metodo per la sintesi di due trisolfuri ciclici, 1,2,3-tritiano 11 e 2,3,4-benzotritiepina 12 dai sali bifunzionali di Bunte 9 e 10, rispettivamente. I sali di Bunte sono stati fatti reagire con solfuro di sodio in presenza di formaldeide che ha dato 11 e 12 (Schema 18). Un sottoprodotto è formato come composto polimerico [74]. La purezza dei prodotti è stata migliorata con l'aggiunta di formaldeide nella miscela di reazione perché si combina con il solfito e minimizza la formazione di disolfuri da trisolfuri.