marco the chemistry
2013-03-15 17:31
Solitamente non faccio molte sintesi organiche, però ultimamente mi sto avvicinando alla chimica organica pratica! La sintesi qui descritta è quella di una base di Schiff (immina secondaria), che è anche un legante per metalli di transizione.
Materiali:
- acetilacetone
- etilendiamina
- vetreria base
Materiali:
In un becker o un palloncino si pongono 21ml di acetilacetone (eccesso) e un'ancoretta magnetica, si accende l'agitazione magnetica e si aggiungono lentamente 6,6ml di etilendiamina tramite imbuto gocciolatore o semplicemente pipetta graduata munita di pipettatore che tiene bene. Alle prima aggiunte si noterà la formazione di un solido bianco, ma man mano che l'etilendiamina viene aggiunta, il calore di reazione porta a fusione la massa e fa evaporare via l'acqua sviluppata come sottoprodotto. Si formerà un liquido giallognolo che per raffreddamento si rapprende in una massa biancastra.

 Nell'articolo che ho trovato erano consigliate due ricristallizzazioni da acqua, ma non era specificato il volume di solvente da utilizzare. Ho visto che un buon compromesso è utilizzare 40 ml di acqua. Si aggiungono quindi circa 40ml di acqua alla miscela fredda e si scalda su piastra fino a che tutto il solido non si è dissolto a dare una soluzione limpida e giallina. La molecola è molto solubile in acqua calda, poco in acqua fredda. Quando tutto si è dissolto, si procede come per una normale cristallizzazione e, al raffreddamento si ottiene una massa quasi solida di un bel colore bianco, appena sporcato di giallino. Si filtra su bukner e si lava con poca acqua, le acqua di lavaggio diventano gialline, mentre il solido nell'imbuto rimane bianco candido.
Nell'articolo che ho trovato erano consigliate due ricristallizzazioni da acqua, ma non era specificato il volume di solvente da utilizzare. Ho visto che un buon compromesso è utilizzare 40 ml di acqua. Si aggiungono quindi circa 40ml di acqua alla miscela fredda e si scalda su piastra fino a che tutto il solido non si è dissolto a dare una soluzione limpida e giallina. La molecola è molto solubile in acqua calda, poco in acqua fredda. Quando tutto si è dissolto, si procede come per una normale cristallizzazione e, al raffreddamento si ottiene una massa quasi solida di un bel colore bianco, appena sporcato di giallino. Si filtra su bukner e si lava con poca acqua, le acqua di lavaggio diventano gialline, mentre il solido nell'imbuto rimane bianco candido.
 Si procede ad un'altra cristallizzazione per avere un prodotto più puro, ma questa volta anche la soluzione calda sarà incolore.
Quando tutto è cristallizzato si filtra nuovamente su bukner e si fa asciugare all'aria o su un calorifero. Il composto si presenta come aghi setosi bianco candido, dalla consistenza sembra amianto. Resa 55% (la fonte ne otteneva il 60%).
Si procede ad un'altra cristallizzazione per avere un prodotto più puro, ma questa volta anche la soluzione calda sarà incolore.
Quando tutto è cristallizzato si filtra nuovamente su bukner e si fa asciugare all'aria o su un calorifero. Il composto si presenta come aghi setosi bianco candido, dalla consistenza sembra amianto. Resa 55% (la fonte ne otteneva il 60%).
 Allego il pdf dell'articolo utilizzato come fonte.
Adesso sarebbe interessante preparare qualche complesso con qualche bel metallo di transizione. So che esistono i complessi [Ni acen], [Cu acen], [Co acen], [Mn X acen] con X=Cl, Br, I, NCS, ecc e [Co acen (amina)2]X, con X come per il Mn. Solo che non ho ancora trovato una metodica seria e che usi solventi reperibili....Non si trova molto in rete riguardo a questa molecola.
Anche nel pdf qui allegato si parla della sintesi di qualche complesso, peccato che si siano scrodati di scrivere che solvente utilizzare...
Allego il pdf dell'articolo utilizzato come fonte.
Adesso sarebbe interessante preparare qualche complesso con qualche bel metallo di transizione. So che esistono i complessi [Ni acen], [Cu acen], [Co acen], [Mn X acen] con X=Cl, Br, I, NCS, ecc e [Co acen (amina)2]X, con X come per il Mn. Solo che non ho ancora trovato una metodica seria e che usi solventi reperibili....Non si trova molto in rete riguardo a questa molecola.
Anche nel pdf qui allegato si parla della sintesi di qualche complesso, peccato che si siano scrodati di scrivere che solvente utilizzare... Stavo quasi pensando di usare le stesse procedure utilizzate per preparare i complessi con l'H2salen, cambiando ovviamente la base di Schiff.
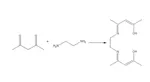
Ecco la reazione che porta alla formazione del composto, ho tralasciato l'acqua che si forma come sottoprodotto.
Stavo quasi pensando di usare le stesse procedure utilizzate per preparare i complessi con l'H2salen, cambiando ovviamente la base di Schiff.
Ecco la reazione che porta alla formazione del composto, ho tralasciato l'acqua che si forma come sottoprodotto.

I seguenti utenti ringraziano marco the chemistry per questo messaggio: ale93, Mario, fosgene, quimico, Max Fritz