marco the chemistry
2014-08-26 07:57
Materiali:
- anidride isatoica
- metanolo
- sodio idrossido
- etere etilico
- apparato per riflusso e distillazione frazionata
Procedimento:
La preparazione di questo estere è un po' diversa da quelle viste fino ad ora, infatti la classica esterificazione di Fisher non viene molto bene poichè l'amino gruppo dell'acido antranilico viene protonato dal catalizzatore acido e la reazione non parte... bisognerebbe usare 1,1 equivalenti di H2SO4, ma poi si incontrano altre difficoltà succesive. Ho quindi preferito utilizzare un'altra via di sintesi, molto più semplice e lineare!
In un pallone da 250ml si pongono 0,3g di NaOH e 18,3ml di MeOH, si agita scaldando fino a quando tutta la base non si è dissolta, si aggiungono quindi 24,4g di anidride isatoica. Si monta il condensatore a ricadere e si pone il palloncino in un bagno di acqua a circa 70°, ben presto comincia l'evoluzione di CO2, segno che la reazione sta procedendo per bene, dopo circa 30 minuti la miscela si è trasformata in un soluzione marrone limpida.
Si fa raffreddare e si aggiungono 100ml circa di acqua: precipita subito uno strato oleoso più denso della fase acquosa e colorato in marrone. Per estrarre il prodotto il più possibile si aggiungono 100ml circa di etere etilico e si separa in imbuto separatore, purtroppo la miscela bifasica tende a formare odiose emulsioni, ma con un po' di pazienza si riesce a separare bene la fase organica. Altra cosa interessante è che praticamente tutto il colore marrone passa dalla fase organica alla fase acquosa quando si aggiunge il solvente organico.
Una volta separata, questa viene lavata con acqua (adesso non si formano più emulsioni) e seccata su CaCl2, l'etere viene quindi distillato a bagno maria bollente lasciando nel pallone un residuo marrone chiaro molto profumato.
Questo infine viene distillato raccogliendo ciò che bolle intorno a 256°, praticamente tutto il contenuto del pallone passa in questo intervallo, rimane solo un piccolo residuo nero che viene eliminato. Dopo distillazione ho ottenuto 14,6g (65% del teorico) di prodotto purificato che si presenta come un liquido molto viscoso e praticamente incolore che solidifica formando una massa bianca untuosa se lasciato in freezer per un poco.
L'aroma di questo estere può essere apprezzato bene solo quando la sostanza viene diluita notevolmente: ha un buonissimo aroma molto florealee e che ricorda il profumo dei fiori di agrumi, con una nota anche di ylang ylang.
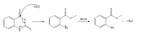
Vediamo ora un po' di meccanismo di reazione: l'anidride isatoica viene attaccata da un nucleofilo (in questo caso MeO- generato da MeOH e NaOH) sul carbonio 4, questo attacco produce eliminazione di CO2 gassosa e la formazione dell'estere con il gruppo aminico deprotonato, questa base molto forte estrae un protone dal solvente (MeOH), rigenerando il metossido. Dato che si lavora con basi molto forti è bene eliminare più acqua possibile, utilizzando magari metanolo assoluto.
La sintesi è stata presa dall'articolo qui allegato.
Per la prossima volta voglio provare a condensare l'anidride isatoica con anilina e acetilacetone per tentare la sintesi di un chinazolone.
I seguenti utenti ringraziano marco the chemistry per questo messaggio: ohilà, fosgene, TrevizeGolanCz, al-ham-bic, quimico, zodd01









 Visto che non ho il metanolo, mi chiedevo se si potesse fare nello stesso modo l'estere etilico.
Da quel che leggo nell'articolo, però, l'EtOH 95% contiene troppa acqua, o sbaglio? Andrebbe anidrificato...
Visto che non ho il metanolo, mi chiedevo se si potesse fare nello stesso modo l'estere etilico.
Da quel che leggo nell'articolo, però, l'EtOH 95% contiene troppa acqua, o sbaglio? Andrebbe anidrificato...