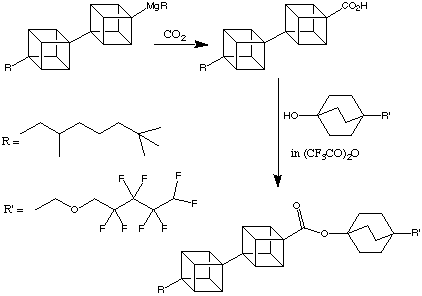
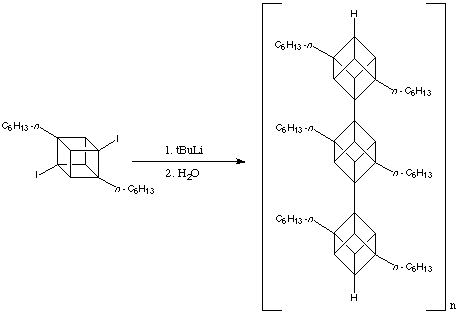
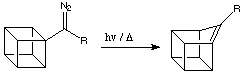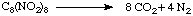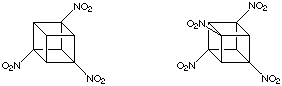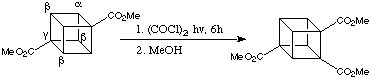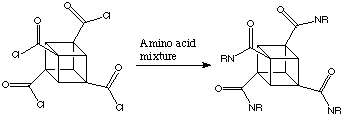Sin dalla prima sintesi del cubano, è stata prodotta un'impressionante gamma di conoscenze ed interpretazioni che hanno portato alla preparazione di molti differenti derivati del cubano amassed.
La reattività del cubano e dei suoi derivati può essere illustrata studiando la sua reattività e i metodi per sintetizzare specifiche molecole bersaglio. Le reazioni possono essere divise in due grandi categorie:
1. Trasformazioni di gruppi funzionali
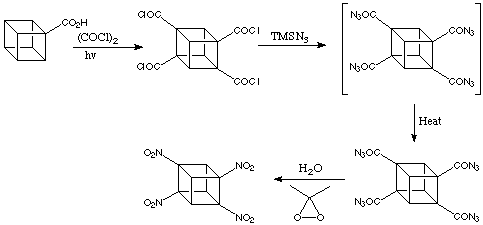
È stato già menzionato che i gruppi carbossilici dell'acido cubane-1,4-dicarbossilico, come la maggior parte degli altri gruppi funzionali sul cubano, sono straordinariamente ben tollerati. La maggior parte delle tipiche trasformazioni di gruppi funzionali possono essere fatte con successo. Questa cosa può essere apprezzata nella preparazione dell'1,4-dinitrocubano messa a puto a Chicago da Shankar et al nel 1984.
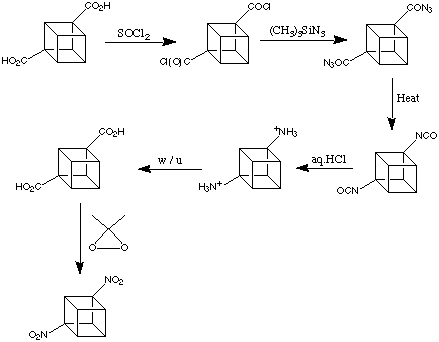
Qui, sono usate moderne versioni della metodologia classica. Queste conversioni sono facili da fare sul cubano come su un classico acido carbossilico. Notate, così come per la maggior parte dei cubani, che l'intermedio cubil-1,4-diisocianato nello schema di reazione è un materiale stabile, cristallino (m.p. 112-114 °C).
L'1,4-dinitrocubano, il prodotto finale, è perfettamente facile da maneggiare. Esso è meno sensibile per shock del TNT e notevolmente stabile termicamente (decompone a 260 °C).
2. Sostituzione sulla struttura del cubano
Le trasformazioni di gruppi funzionali sono utli per la preparazione di molti cubani mono- e disostituiti, dato che i corrispondenti acidi carbossilici sono facilmente disponibili. Ma questo non è abbastanza per la preparazioni di cubani più sostituiti. Come Reddy et al. hanno mostrato, la sostituzione del cubano tramite radicale cubile è abbastanza facile. Comunque, come è solitamente il caso con reazioni radicaliche, sono ottenute miscele di prodotti. La iodurazione luce indotta del cubano con t-butil ipoiodito porta a mono-, di-, triiodocubani, etc.
La sfida è ottenere una sostituzione sistematica e controllata sulla struttura del cubano.
Elencherò ora alcuni esempi di reazioni di sostituzione sul cubano.
Attivazione dell'ammide per orto metallazione
L'idea chiave qui fu di usare l'attivazione del gruppo vicinale per assistere la metallazione del cubano. In relazione a questa era ben noto che un sostituente ammidico su un arene facilitava la litiazione in posizione orto tramite attivazione dell'atomo di idrogeno dell'arene.
Ci sono alcune somiglianze tra cubani ed areni: entrambi hanno un legame C-H con un aumentato carattere s, ed in entrambi i sostituenti adiacenti (orto) sono forzati ad essere coplanari.
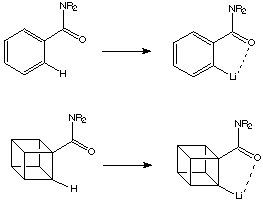
Quindi era fu supposto che potesse essere possibile litiare cubanammidi.
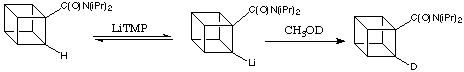
Il lavoro determinante fu fatto da Graziano Castaldi all'Eaton Lab nel 1985. Mostrò che una piccola concentrazione all'equilibrio di derivato orto litiato (centro, sotto) è formata effettivamente quando la diisopropilammide dell'acido cubanocarbossilico è trattata con un grande eccesso di una forte base, non nucleofila come la ltio tetrametilpiperidide (LiTMP). Quando la miscela di reazioni è
quenchata con CH
3OD la cubanammide recuperata contiene approssimativamente il 3% di deuterio in posizione 2 (orto); il materiale dideuterato non dovrebbe esser rivelato.
 Transmetallazione
Transmetallazione
Nel passaggio chiave successivo, Castaldi mostrò la transmetallazione essere il passaggio dorato successivo nella sintesi di cubani sostituiti. Quando la litiazione di una cubanammide è condotto in presenza di sali di mercurio, il composto di litio formato prima è rapidamente mercurato, ed il legame molto polare C-Li è sostituito dal legame C-Hg molto vicino alla covalenza. In questo modo, lo starting material nello schema sotto può essere completamente convertito in un cubano metallato.
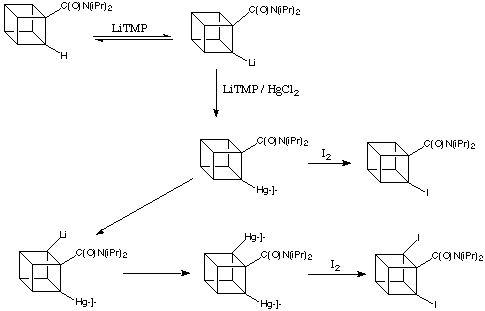
Il gruppo ammidico è importante nello stabilire l'intermedio litiato del cubano, ma non il composto mercurato. Non appena il litio viene sostituito dal mercurio, il gruppo ammidico è ancora in grado di assistere la rimozione di un altro idrogeno in orto, e il processo può continuare.
Metallazione/transmetallazione è la base di una completa metodologia sintetica per la preparazione di una grande varietà di cubani sostituiti. I cubani mercurati sono utili per la formazioni di alogenocubani, dato che il legame C-Hg è rotto facilmente da alogeni come lo iodio.
Reagenti di Grignard contenenti il cubile
Bashir-Hashimi al Geo-Centres introdusse la transmetallazione con sali di magnesio e così fornì un facile accesso ai reagenti mono- e bis-Grignard contenenti il cubile. La conversione procedeva tramite litiazione/bromomagnesiazione un passo alla volta. La seconda metallazione del cubano avviene in una posizione lontana dalla prima - abbastanza comprensibile considerando le polarità degli intermedi. La successiva metallazione non avveniva. Nella maggior parte dei casi, la conversione totale di queste reazioni è staordinariamente buona; nell'esempio mostrato sotto rese del 90-95% sono facili da ottenere sia in produzioni su piccola che grande scala.
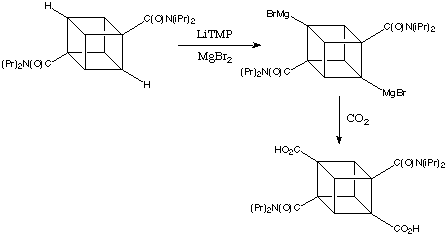 Orto magnesiazione
Orto magnesiazione
Durante l'ampliamento della sintesi dei cubani con differenti schemi di sostituzione, il gruppo di Eaton trovò che il trattamento della 2,4-dicianocubanammide con LiTMP portava a due acidi cubano-carbossilici isomerici tetrasostituiti dopo carbossilazione.
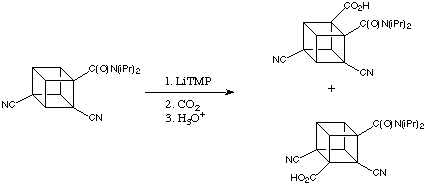
Gli effetti elettron-attrattori dei gruppi ciano assieme all'amide stabilizzano entrambi gli intermedi litiati del cubano così bene che solo un leggereo eccesso di LiTMP è necessario per ottenere una deprotonazione abbastanza completa anche a -78 °C. Nell'iniziale step di litiazione, l'attivazione del legame C-H del cubano tramite i due gruppi ciano che sia affiancano competono per l'orto attivazione data da un gruppo ammidico. Questo porta a litiazioni competitive e ad una miscela di prodotti.
Nel tentativo di ottenere maggiore selettività in questa reazione, fu esaminato l'effetto dell'aggiunta di MgBr
2. Quando il rapporto tra LiTMP e MgBr
2 fu 1.5:1, il rapporto tra prodotti fu aumentato a 9:1 favorendo la carbossilazione in orto alla funzione ammidica. Questo suggerì un'importante e precendemente non prevista reazione: la diretta magnesiazione tramite TMPMgBr (un base di Hauser) e/o tramite (TMP)
2Mg. Questa idea è stata ora ampliata in un nuovo potente processo soprannominato orto magnesiazione ed è stato succesivamente trovato che le basi magnesio ammide sono estremamente utili in sintesi.
Quando la dicianocubanammide (sotto) è trattata con TMPMgBr o (TMP)
2Mg l'unico prodotto dopo carbossilazione (90% di resa!) è quello che contiene il gruppo carbossilico vicino al gruppo ammidico attivante.
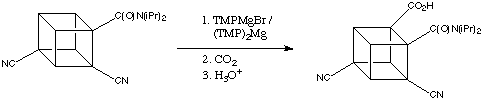
Questa reazione procede bene anche a -78 °C. L'effetto induttivo del gruppo ciano chiaramente migliora la reazione, ma il gruppo ciano stesso non dirige in orto la magnesiazione.
Schemi alternativi di sostituzione
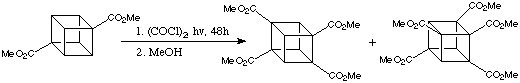
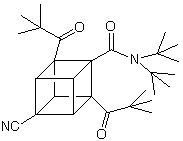
Sebbene l'attivazione di un singolo gruppo ammidico sia sufficiente per la metallazione dei cubani, la presenza di ulteriori gruppi elettron-attrattori aumenta la reattività enormemente. La 4-cianocubanammide è molto più reattiva dell'ammide non sostituita. In casi quando l'elettrofilo può coesistere con la base è possibile sostituire tutte tre le posizioni in orto all'amide in una reazione straordinariamente semplice,
one-pot che procede tramite successive metallazioni. Quindi, per esempio, la 4-cianocubanammide può essere convertita direttamente nel derivato tri(t-butilcarbonile).
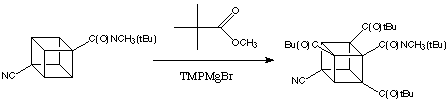
Dato che l'ossidazione di Baeyer-Villiger di t-butil cubil chetoni è completamente specifica - solo il gruppo t-butile migra - il trichetone (sotto) può essere facilmente convertito a cubano policarbossilato:
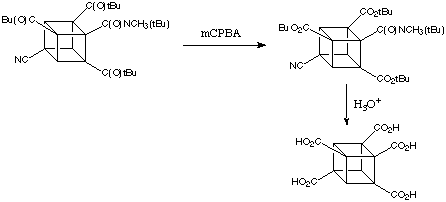
È giusto dire che quasi qualsiasi combinazione o permutazione di gruppi funzionali e posizioni sul nucleo cubano possono essere ottenute ora tramite una chimica abbastanza semplice.
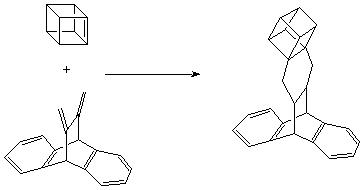
Il grupo di Eaton ha anche sintetizzato i cubani con anelli eterociclici fusi; un esempio di questo è mostrato sotto.
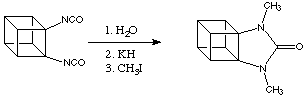
Abbastanza diversi dalle aspettative questi "eteropropellano cubani" sono notevolmente stabili. Gli atomi di azoto possono essere alchilati o ntirati senza interferenza da parte di reazioni d'apertura d'anello. È interessante notare che il legame C-C condiviso dall'urea ed il sistema cubano è sostanzialmente più corto di un legame equivalente in cubani o uree cicliche. L'origine di questo effetto non è conosciuta.
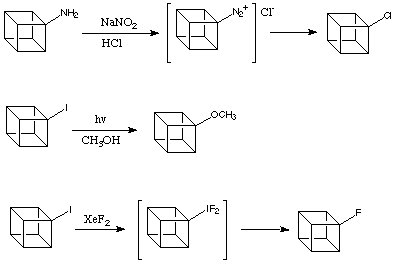
Il cation cubile
Una delle più grandi sorprese nella ricerca sul cubano fu la scoperta che il catione cubile è molto più accessibile di quanto aspettato. Ogni cosa circa il catione cubile sembrava sfavorevole:
* la geometria riguardo il catione carico positivamente è molto lontana dalla planarità,
* gli orbitali esociclici nel cubano sono s-ricchi,
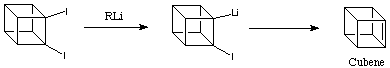
* la stabilizzazione iperconiugativa dovrebbe richiedere strutture ad elevata energia, tipo cubene.
Calcoli ab-initio (6-31G*, senza correlazione elettronica) posizionano il catione cubile circa 20 kcal/mol più in alto in energia del t-butil catione e circa 5 kcal/mol più in alto in energia del carbione 1-norbornile.
 Il fascino della chimica del cubano è continuato con la stessa forza sin dalla inaugurale costruzione del nucleo di cubano fatta da Eaton e Cole nel 1964.
Da una veloce ricerca della letteratura del cubano è ovvio che il pioniere nella sua sintesi e successiva sostituzione fu Philip E. Eaton.
I cubani hanno trovato applicazioni in diverse aree scientifiche, incluse:
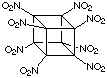
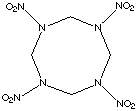
* esplosivi ad elevata densità,
* propellenti,
* farmaci,
* polimeri.
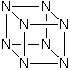
È stato anche ipotizzato che l'analogo del cubano, l'ottaazacubano (N8), se formato dovrebbe essere stabile. Mentre è proposto che sarebbe altamente instabile termodinamicamente, la sua decomposizione ad N2 è proibita dalla simmetria orbitalica, nella stessa maniera del cubano.
Il fascino della chimica del cubano è continuato con la stessa forza sin dalla inaugurale costruzione del nucleo di cubano fatta da Eaton e Cole nel 1964.
Da una veloce ricerca della letteratura del cubano è ovvio che il pioniere nella sua sintesi e successiva sostituzione fu Philip E. Eaton.
I cubani hanno trovato applicazioni in diverse aree scientifiche, incluse:
* esplosivi ad elevata densità,
* propellenti,
* farmaci,
* polimeri.
È stato anche ipotizzato che l'analogo del cubano, l'ottaazacubano (N8), se formato dovrebbe essere stabile. Mentre è proposto che sarebbe altamente instabile termodinamicamente, la sua decomposizione ad N2 è proibita dalla simmetria orbitalica, nella stessa maniera del cubano.
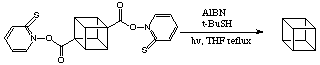
 hai mai provato ad eseguirne la sintesi????? mi rendo conto che non sia una cosa banale....però sembrerebbe tentabile....anche se come scrivi tu anche molto costoso!
hai mai provato ad eseguirne la sintesi????? mi rendo conto che non sia una cosa banale....però sembrerebbe tentabile....anche se come scrivi tu anche molto costoso!
 Quindi era fu supposto che potesse essere possibile litiare cubanammidi.
Il lavoro determinante fu fatto da Graziano Castaldi all'Eaton Lab nel 1985. Mostrò che una piccola concentrazione all'equilibrio di derivato orto litiato (centro, sotto) è formata effettivamente quando la diisopropilammide dell'acido cubanocarbossilico è trattata con un grande eccesso di una forte base, non nucleofila come la ltio tetrametilpiperidide (LiTMP). Quando la miscela di reazioni è quenchata con CH3OD la cubanammide recuperata contiene approssimativamente il 3% di deuterio in posizione 2 (orto); il materiale dideuterato non dovrebbe esser rivelato.
Quindi era fu supposto che potesse essere possibile litiare cubanammidi.
Il lavoro determinante fu fatto da Graziano Castaldi all'Eaton Lab nel 1985. Mostrò che una piccola concentrazione all'equilibrio di derivato orto litiato (centro, sotto) è formata effettivamente quando la diisopropilammide dell'acido cubanocarbossilico è trattata con un grande eccesso di una forte base, non nucleofila come la ltio tetrametilpiperidide (LiTMP). Quando la miscela di reazioni è quenchata con CH3OD la cubanammide recuperata contiene approssimativamente il 3% di deuterio in posizione 2 (orto); il materiale dideuterato non dovrebbe esser rivelato.
 Transmetallazione
Nel passaggio chiave successivo, Castaldi mostrò la transmetallazione essere il passaggio dorato successivo nella sintesi di cubani sostituiti. Quando la litiazione di una cubanammide è condotto in presenza di sali di mercurio, il composto di litio formato prima è rapidamente mercurato, ed il legame molto polare C-Li è sostituito dal legame C-Hg molto vicino alla covalenza. In questo modo, lo starting material nello schema sotto può essere completamente convertito in un cubano metallato.
Transmetallazione
Nel passaggio chiave successivo, Castaldi mostrò la transmetallazione essere il passaggio dorato successivo nella sintesi di cubani sostituiti. Quando la litiazione di una cubanammide è condotto in presenza di sali di mercurio, il composto di litio formato prima è rapidamente mercurato, ed il legame molto polare C-Li è sostituito dal legame C-Hg molto vicino alla covalenza. In questo modo, lo starting material nello schema sotto può essere completamente convertito in un cubano metallato.
 Il gruppo ammidico è importante nello stabilire l'intermedio litiato del cubano, ma non il composto mercurato. Non appena il litio viene sostituito dal mercurio, il gruppo ammidico è ancora in grado di assistere la rimozione di un altro idrogeno in orto, e il processo può continuare.
Metallazione/transmetallazione è la base di una completa metodologia sintetica per la preparazione di una grande varietà di cubani sostituiti. I cubani mercurati sono utili per la formazioni di alogenocubani, dato che il legame C-Hg è rotto facilmente da alogeni come lo iodio.
Reagenti di Grignard contenenti il cubile
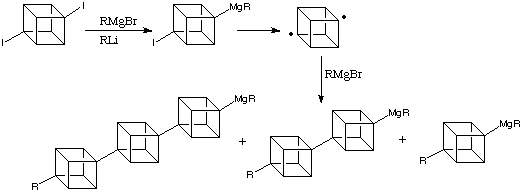
Bashir-Hashimi al Geo-Centres introdusse la transmetallazione con sali di magnesio e così fornì un facile accesso ai reagenti mono- e bis-Grignard contenenti il cubile. La conversione procedeva tramite litiazione/bromomagnesiazione un passo alla volta. La seconda metallazione del cubano avviene in una posizione lontana dalla prima - abbastanza comprensibile considerando le polarità degli intermedi. La successiva metallazione non avveniva. Nella maggior parte dei casi, la conversione totale di queste reazioni è staordinariamente buona; nell'esempio mostrato sotto rese del 90-95% sono facili da ottenere sia in produzioni su piccola che grande scala.
Il gruppo ammidico è importante nello stabilire l'intermedio litiato del cubano, ma non il composto mercurato. Non appena il litio viene sostituito dal mercurio, il gruppo ammidico è ancora in grado di assistere la rimozione di un altro idrogeno in orto, e il processo può continuare.
Metallazione/transmetallazione è la base di una completa metodologia sintetica per la preparazione di una grande varietà di cubani sostituiti. I cubani mercurati sono utili per la formazioni di alogenocubani, dato che il legame C-Hg è rotto facilmente da alogeni come lo iodio.
Reagenti di Grignard contenenti il cubile
Bashir-Hashimi al Geo-Centres introdusse la transmetallazione con sali di magnesio e così fornì un facile accesso ai reagenti mono- e bis-Grignard contenenti il cubile. La conversione procedeva tramite litiazione/bromomagnesiazione un passo alla volta. La seconda metallazione del cubano avviene in una posizione lontana dalla prima - abbastanza comprensibile considerando le polarità degli intermedi. La successiva metallazione non avveniva. Nella maggior parte dei casi, la conversione totale di queste reazioni è staordinariamente buona; nell'esempio mostrato sotto rese del 90-95% sono facili da ottenere sia in produzioni su piccola che grande scala.
 Orto magnesiazione
Durante l'ampliamento della sintesi dei cubani con differenti schemi di sostituzione, il gruppo di Eaton trovò che il trattamento della 2,4-dicianocubanammide con LiTMP portava a due acidi cubano-carbossilici isomerici tetrasostituiti dopo carbossilazione.
Orto magnesiazione
Durante l'ampliamento della sintesi dei cubani con differenti schemi di sostituzione, il gruppo di Eaton trovò che il trattamento della 2,4-dicianocubanammide con LiTMP portava a due acidi cubano-carbossilici isomerici tetrasostituiti dopo carbossilazione.
 Gli effetti elettron-attrattori dei gruppi ciano assieme all'amide stabilizzano entrambi gli intermedi litiati del cubano così bene che solo un leggereo eccesso di LiTMP è necessario per ottenere una deprotonazione abbastanza completa anche a -78 °C. Nell'iniziale step di litiazione, l'attivazione del legame C-H del cubano tramite i due gruppi ciano che sia affiancano competono per l'orto attivazione data da un gruppo ammidico. Questo porta a litiazioni competitive e ad una miscela di prodotti.
Nel tentativo di ottenere maggiore selettività in questa reazione, fu esaminato l'effetto dell'aggiunta di MgBr2. Quando il rapporto tra LiTMP e MgBr2 fu 1.5:1, il rapporto tra prodotti fu aumentato a 9:1 favorendo la carbossilazione in orto alla funzione ammidica. Questo suggerì un'importante e precendemente non prevista reazione: la diretta magnesiazione tramite TMPMgBr (un base di Hauser) e/o tramite (TMP)2Mg. Questa idea è stata ora ampliata in un nuovo potente processo soprannominato orto magnesiazione ed è stato succesivamente trovato che le basi magnesio ammide sono estremamente utili in sintesi.
Quando la dicianocubanammide (sotto) è trattata con TMPMgBr o (TMP)2Mg l'unico prodotto dopo carbossilazione (90% di resa!) è quello che contiene il gruppo carbossilico vicino al gruppo ammidico attivante.
Gli effetti elettron-attrattori dei gruppi ciano assieme all'amide stabilizzano entrambi gli intermedi litiati del cubano così bene che solo un leggereo eccesso di LiTMP è necessario per ottenere una deprotonazione abbastanza completa anche a -78 °C. Nell'iniziale step di litiazione, l'attivazione del legame C-H del cubano tramite i due gruppi ciano che sia affiancano competono per l'orto attivazione data da un gruppo ammidico. Questo porta a litiazioni competitive e ad una miscela di prodotti.
Nel tentativo di ottenere maggiore selettività in questa reazione, fu esaminato l'effetto dell'aggiunta di MgBr2. Quando il rapporto tra LiTMP e MgBr2 fu 1.5:1, il rapporto tra prodotti fu aumentato a 9:1 favorendo la carbossilazione in orto alla funzione ammidica. Questo suggerì un'importante e precendemente non prevista reazione: la diretta magnesiazione tramite TMPMgBr (un base di Hauser) e/o tramite (TMP)2Mg. Questa idea è stata ora ampliata in un nuovo potente processo soprannominato orto magnesiazione ed è stato succesivamente trovato che le basi magnesio ammide sono estremamente utili in sintesi.
Quando la dicianocubanammide (sotto) è trattata con TMPMgBr o (TMP)2Mg l'unico prodotto dopo carbossilazione (90% di resa!) è quello che contiene il gruppo carbossilico vicino al gruppo ammidico attivante.
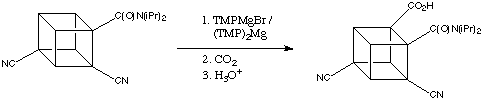 Questa reazione procede bene anche a -78 °C. L'effetto induttivo del gruppo ciano chiaramente migliora la reazione, ma il gruppo ciano stesso non dirige in orto la magnesiazione.
Schemi alternativi di sostituzione
Sebbene l'attivazione di un singolo gruppo ammidico sia sufficiente per la metallazione dei cubani, la presenza di ulteriori gruppi elettron-attrattori aumenta la reattività enormemente. La 4-cianocubanammide è molto più reattiva dell'ammide non sostituita. In casi quando l'elettrofilo può coesistere con la base è possibile sostituire tutte tre le posizioni in orto all'amide in una reazione straordinariamente semplice, one-pot che procede tramite successive metallazioni. Quindi, per esempio, la 4-cianocubanammide può essere convertita direttamente nel derivato tri(t-butilcarbonile).
Questa reazione procede bene anche a -78 °C. L'effetto induttivo del gruppo ciano chiaramente migliora la reazione, ma il gruppo ciano stesso non dirige in orto la magnesiazione.
Schemi alternativi di sostituzione
Sebbene l'attivazione di un singolo gruppo ammidico sia sufficiente per la metallazione dei cubani, la presenza di ulteriori gruppi elettron-attrattori aumenta la reattività enormemente. La 4-cianocubanammide è molto più reattiva dell'ammide non sostituita. In casi quando l'elettrofilo può coesistere con la base è possibile sostituire tutte tre le posizioni in orto all'amide in una reazione straordinariamente semplice, one-pot che procede tramite successive metallazioni. Quindi, per esempio, la 4-cianocubanammide può essere convertita direttamente nel derivato tri(t-butilcarbonile).
 Dato che l'ossidazione di Baeyer-Villiger di t-butil cubil chetoni è completamente specifica - solo il gruppo t-butile migra - il trichetone (sotto) può essere facilmente convertito a cubano policarbossilato:
Dato che l'ossidazione di Baeyer-Villiger di t-butil cubil chetoni è completamente specifica - solo il gruppo t-butile migra - il trichetone (sotto) può essere facilmente convertito a cubano policarbossilato:
 È giusto dire che quasi qualsiasi combinazione o permutazione di gruppi funzionali e posizioni sul nucleo cubano possono essere ottenute ora tramite una chimica abbastanza semplice.
Il grupo di Eaton ha anche sintetizzato i cubani con anelli eterociclici fusi; un esempio di questo è mostrato sotto.
È giusto dire che quasi qualsiasi combinazione o permutazione di gruppi funzionali e posizioni sul nucleo cubano possono essere ottenute ora tramite una chimica abbastanza semplice.
Il grupo di Eaton ha anche sintetizzato i cubani con anelli eterociclici fusi; un esempio di questo è mostrato sotto.
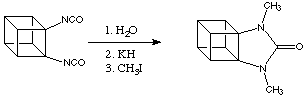 Abbastanza diversi dalle aspettative questi "eteropropellano cubani" sono notevolmente stabili. Gli atomi di azoto possono essere alchilati o ntirati senza interferenza da parte di reazioni d'apertura d'anello. È interessante notare che il legame C-C condiviso dall'urea ed il sistema cubano è sostanzialmente più corto di un legame equivalente in cubani o uree cicliche. L'origine di questo effetto non è conosciuta.
Il cation cubile
Una delle più grandi sorprese nella ricerca sul cubano fu la scoperta che il catione cubile è molto più accessibile di quanto aspettato. Ogni cosa circa il catione cubile sembrava sfavorevole:
* la geometria riguardo il catione carico positivamente è molto lontana dalla planarità,
* gli orbitali esociclici nel cubano sono s-ricchi,
* la stabilizzazione iperconiugativa dovrebbe richiedere strutture ad elevata energia, tipo cubene.
Calcoli ab-initio (6-31G*, senza correlazione elettronica) posizionano il catione cubile circa 20 kcal/mol più in alto in energia del t-butil catione e circa 5 kcal/mol più in alto in energia del carbione 1-norbornile.
Abbastanza diversi dalle aspettative questi "eteropropellano cubani" sono notevolmente stabili. Gli atomi di azoto possono essere alchilati o ntirati senza interferenza da parte di reazioni d'apertura d'anello. È interessante notare che il legame C-C condiviso dall'urea ed il sistema cubano è sostanzialmente più corto di un legame equivalente in cubani o uree cicliche. L'origine di questo effetto non è conosciuta.
Il cation cubile
Una delle più grandi sorprese nella ricerca sul cubano fu la scoperta che il catione cubile è molto più accessibile di quanto aspettato. Ogni cosa circa il catione cubile sembrava sfavorevole:
* la geometria riguardo il catione carico positivamente è molto lontana dalla planarità,
* gli orbitali esociclici nel cubano sono s-ricchi,
* la stabilizzazione iperconiugativa dovrebbe richiedere strutture ad elevata energia, tipo cubene.
Calcoli ab-initio (6-31G*, senza correlazione elettronica) posizionano il catione cubile circa 20 kcal/mol più in alto in energia del t-butil catione e circa 5 kcal/mol più in alto in energia del carbione 1-norbornile.